Archive for Agustus 2011
Sifat Protektif Teh Hijau Terungkap

"Kami juga menemukan bahwa pencernaan senyawa ini memiliki sifat anti-kanker, secara signifikan memperlambat pertumbuhan sel tumor."
Minum teh hijau secara teratur bisa melindungi otak terhadap perkembangan Alzheimer dan bentuk demensia lain, demikian menurut penelitian terbaru oleh para ilmuwan di Universitas Newcastle.
Penelitian yang diterbitkan dalam jurnal akademis Phytomedicine, juga menyarankan bahwa obat Cina kuno ini dapat memainkan peran penting dalam melindungi tubuh terhadap kanker.
Dipimpin oleh Dr. Ed Okello, tim Newcastle ingin tahu apakah sifat protektif teh hijau masih aktif begitu teh telah dicerna.
Pencernaan adalah sebuah proses penting yang memberi tubuh kita nutrisi yang kita butuhkan untuk bertahan hidup. Tapi, kata Dr. Okello, meskipun asupan yang masuk ke dalam mulut kita secara umum mengandung sifat yang meningkatkan kesehatan, kita tidak bisa menganggap senyawa tersebut akan bisa terserap oleh tubuh.
“Apa yang benar-benar menarik tentang studi ini, kami menemukan bahwa bila teh hijau dicerna oleh enzim dalam usus, zat kimia yang dihasilkan sebenarnya lebih efektif terhadap pemicu utama pengembangan Alzheimer daripada bentuk teh yang tercerna,” jelas Dr. Okello, yang berbasis di Sekolah Pertanian, Pangan dan Pembangunan Pedesaan di Universitas Newcastle.
“Selain itu, kami juga menemukan bahwa pencernaan senyawa ini memiliki sifat anti-kanker, secara signifikan memperlambat pertumbuhan sel tumor yang kami gunakan dalam percobaan kami.”
Sebagai bagian dari penelitian ini, tim Newcastle bekerjasama dengan Dr. Gordon McDougall dari Group Produk Tanaman Pangan dan Mutu di Skotlandia Crop Research Institute di Dundee, yang mengembangkan teknologi yang mensimulasikan sistem pencernaan manusia.
Hal inilah yang memungkinkan tim riset menganalisis sifat protektif dari produk pencernaan.
Dua senyawa yang diketahui memainkan peran penting dalam perkembangan penyakit Alzheimer – peroksida hidrogen dan protein yang dikenal sebagai beta-amiloid.
Penelitian sebelumnya telah menunjukkan bahwa senyawa yang dikenal sebagai polifenol, terkandung di dalam teh hitam dan hijau, memiliki sifat pelindung saraf, mengikat dengan senyawa beracun dan melindungi sel-sel otak.
Ketika ditelan, polifenol terpecah untuk menghasilkan campuran senyawa dan inilah yang diuji oleh tim Newcastle dalam penelitian terbaru mereka.
“Inilah salah satu alasan mengapa kami harus berhati-hati ketika kami membuat klaim tentang manfaat kesehatan dari berbagai makanan dan suplemen,” jelas Dr. Okello.
“Ada bahan kimia tertentu yang kami tahu akan bermanfaat dan kami bisa mengidentifikasi makanan yang kaya manfaat, namun apa yang terjadi selama proses pencernaan sangat penting untuk mencari tahu apakah makanan ini benar-benar melakukan kegunaannya bagi kita.”
Dengan melakukan percobaan di laboratorium menggunakan model sel tumor, mereka memasukkan sel ini pada konsentrasi yang berbeda-beda dari racun yang berbeda dan senyawa teh hijau yang tercerna.
Dr. Okello menjelaskan, “Bahan kimia tercernanya melindungi sel, mencegah racun dari menghancurkan sel-sel ini.
“Kami juga melihat bahwa mereka mempengaruhi sel-sel kanker, secara signifikan memperlambat pertumbuhan mereka.
“Teh hijau telah digunakan dalam pengobatan tradisional Cina selama berabad-abad dan apa yang kami miliki di sini memberikan bukti ilmiah mengapa hal itu mungkin efektif terhadap beberapa penyakit utama yang kita hadapi saat ini.”
Langkah berikutnya adalah mengetahui apakah senyawa yang bermanfaat ini dihasilkan selama proses pencernaan manusia yang sehat setelah relawan mengkonsumsi polifenol teh. Tim riset ini telah menerima dana dari Biotechnology and Biological Sciences Research Council (BBSRC) untuk penelitian lebih lanjut.
Dr. Okello menambahkan, “Jelas ada banyak faktor yang secara bersamaan memiliki pengaruh terhadap penyakit seperti kanker dan demensia – pola makan yang baik, banyak berolahraga dan gaya hidup sehat, semuanya penting.”
* Sumber artikel: Protective properties of green tea uncovered (ncl.ac.uk)
* Kredit: Newcastle University
* Informasi lebih lanjut: E.J. Okello, G.J. McDougall, S. Kumar, C.J. Seal. In vitro protective effects of colon-available extract of Camellia sinensis (tea) against hydrogen peroxide and beta-amyloid (A?(1–42)) induced cytotoxicity in differentiated PC12 cells. Phytomedicine, 2010; DOI: 10.1016/j.phymed.2010.11.004
Jinten Hitam Biji dari Surga

Selama berabad-abad jintan hitam digunakan jutaan orang di Asia, Timur Tengah, dan Afrika untuk menjaga kesehatan. Minyak dan herbanya diyakini bisa mengobati penyakit yang berhubungan dengan sistem pernapasan, saluran pencernaan, gangguan lambung dan lever serta untuk meningkatkan sistem kekebalan tubuh.
Dominique (36), warga Mampang Prapatan Jakarta Selatan, medio Januari silam, sakit batuk berkepanjangan. Ia mengaku tenggorokannya gatal bukan main. Obat batuk yang biasa dikonsumsi, tak lagi mempan.
Untunglah dari seorang praktisi kesehatan Totok Aura Dian Kenanga di kawasan Kemang, Dominique kemudian mendapat resep minyak jintan hitam, yakni satu sendok teh minyak jintan hitam dicampur dengan segelas kopi. Sehari dua kali, pagi dan malam, selama 2 hari, ia minum campuran itu. Hasilnya, Dominique tak lagi mengalami batuk berkepanjangan.
Lainnya, Patar (45), sudah sebulan mengalami alergi dingin. Bila kedinginan, pria yang tinggal di Bogor ini mengalami gatal-gatal di sekujur.tubuhnya. Ia lalu mengonsumsi 2 kapsul minyak jintan hitam, pagi dan malam. Tiga hari kemudian gatal-gatal itu pun sirna.
Dari Laut Tengah
Jintan hitam dipercaya berasal dari Mediterania (seputar Laut Tengah), sebelum tersebar ke berbagai belahan dunia, termasuk ke Asia. Bentuknya kecil berserabut, ukurannya tidak lebih dari 3 mm. Jintan hitam termasuk dalam keluarga buttercup (Ranunculaceae).
Ada dua jenis tanaman ini, yakni yang berwarna ungu kebiruan dan putih. Orang-orang di tanah Arab telah mengenal Jintan hitam lebih dari 2.000 tahun lalu. Mereka memanfaatkan tanaman ini untuk mengatasi berbagai gangguan kesehatan, misalnya sakit gigi, flu, nyeri sendi.
Di Arab, jintan hitam dikenal sebagai habbatus sauda (biji yang menyenangkan) atau habbatul baraka, artinya biji yang membawa berkah. Bagi kaum muslim, jintan hitam merupakan anugerah Allah. Anjuran Nabi Muhammad SAW untuk memanfaatkan jintan hitam tercatat dalam sebuah hadis.”Tetaplah berobat dengan Habbatus sauda karena sesungguhnya ia bisa mengobati semua penyakit, kecuali kematian.”
Tak heran, tanaman bemama Latin Nigella sativa L. ini masuk dalam daftar obat alami di buku Al-Tibb al-Nabawi atau pengobatan cara Nabi.
Keampuhan jintan hitam menyebar hingga Mesir, Yunani, dan India. Dalam kuburan Tutankhamen ditemukan narasi bahwa jintan hitam dipakai dokter pribadi Firaun sebagai bahan baku minyak dan salep untuk mengobati gangguan pencernaan. Cleopatra dan Nefertiti memakainya untuk merawat kulit agar tetap lembut.
Pada 460 SM, Hippocrates menyarankan penggunaan tanaman ini untuk membangkitkan vitalitas dan energi, kenyamanan, serta mengatasi kelelahan tubuh dan psikis. Dioscoredes, ahli fisika dari Yunani, diabad I melaporkan bahwa jintan hitam dipakai untuk mengobati sakit kepala, hidung tersumbat, sakit gigi, meningkatkan produksi ASI, dan menyembuhkan penyakit internis.
Tahun 980 M, Ibnu Sina dalam The Cannon of Medicine menyatakan Habbatus sauda sebagai perangsang tenaga dan membantu memulihkan kesegaran tubuh, menstimulasi energi, serta membantu penyembuhan dari kelelahan atau kurang semangat.
Kaya Gizi
Tahun 1960, Mahfouz dan Badr EI-Dakhakhny, peneliti Mesir, mengisolasi zat aktif nigellone dari minyak atsiri jintan hitam. Peneliti menemukan, dua minyak volatil (cenderung menguap pada suhu dan tekanan normal) dalam jintan hitam adalah nigellone dan thymoquinone.
Nigellone mencegah terjadinya kejang otot dan melebarkan saluran pernapasan, sehingga jintan hitam berkhasiat untuk penyakit pernapasan. Nigellone juga bersifat antihistamin, sehingga membantu mengurangi alergi, sedangkan thymoquinone berkhasiat antiradang dan antinyeri. Senyawa ini efektif untuk menggelontor racun tubuh.
Di tahun yang sama El-Dakhakhny melaporkan bahwa minyak jintan hitam memiliki kemampuan meredakan radang sendi. Penelitian di laboratorium mengungkapkan kandungan minyak nigellone dan thymoquinone dalam jintan hitam bersifat antileukimia. Penelitian lainnya, kedua unsur itu membantu meningkatkan sistem kekebalan tubuh dan efektif untuk mengobati asma dan batuk kering.
Riset di bidang AIDS dilakukan Dr. Haqpada di Departemen Biologi dan Pusat Penelitian Medis di Riyadh, Arab Saudi, tahun 1997. Hasilnya, jintan hitam mampu meningkatkan rasio sel T positif dan negatif menjadi 55 persen dengan 30 persen aktivitas pembunuh sel alamiah.
Sebuah literatur dari University of Potchefstroom (1989), Afrika Selatan, menjelaskan jintan hitam dapat meningkatkan kadar ASI pada ibu menyusui. Hal ini ditunjukkan oleh kombinasi lipid portion dan struktur hormon dalam habbatus sauda. Menurut Yellia Mangan, penulis buku Cara Bijak Menaklukkan Kanker, jintan hitam kaya akan nutrisi yang mendukung kekebalan tubuh, termasuk
interferon yang membantu penyembuhan kanker.
Tanaman bernama lain black seed ini juga kaya asam lemak tak jenuh dan asam lemak esensial (asam linoleik dan linolenik). Asam alfa -linolenik (omega 3) asam linoleik (omega6), merupakan substansi yang tidak dapat dibentuk di dalam tubuh, sehingga tubuh harus mendapat suplemen yang mengandung kedua asam tersebut.
Jintan hitam juga mengandung 15 macam asam amino, protein, karbohidrat, minyak volatil dan crude fiber. Kandungan vitamin dan mineralnya meliputi kalsium, potasium, besi, magnesium, selenium, vitamin A, B1, B2, B6, C, E dan niacin. Black seed juga mengandung arginine, yang penting pada masa pertumbuhan balita.
Dari Batuk Kering Hingga Kanker
Jintan hitam yang juga dikenal sebagai black car away, black seed, black cumin, shonaiz (Iran), kolonji (Afrika), telah diproduksi dalam bentuk minyak maupun bubuk. Berikut beberapa resep yang ditawarkan Dian Salma dari klinik Dian Kenanga dan herbalis Yellia Mangan:
1. Batuk kering
Bahan : Minyak jintan hitam, air kopi.
Cara : Campur satu sendok teh minyak jintan hitam ke dalam segelas air kopi. Minum 2 kali sehari.
2. Diabetes
Bahan : 1 mangkuk jintan hitam, 1 mangkuk minyak jintan hitam, 1/2 sendok kulit buah delima.
Cara : Hancurkan semua bahan hingga menjadi bubuk. Ambil setengah sendok ramuan tersebut lalu campur dengan minyak jintan hitam. Minum sebelum sarapan selama sebulan.
3. Flu
Bahan : Minyak jintan hitam
Cara : Teteskan 3-4 tetes minyak jintan hitam ke dalam lubang hidung untuk mengurangi penyumbatan pada hidung.
4. Diare
Bahan : Minyak jintan hitam
Cara : Campur 1 sendok makan minyak jintan hitam dengan semangkuk yoghurt. Minum campuran tersebut 2 kali sehari selama tiga hari.
5. Melancarkan ASI
Bahan : 250 g biji jintan hitam, 250 g madu murni.
Cara : Campur biji jintan hitam dan mafu, aduk sampai rata. Minum 2 sendok makan bersama 1 sendok teh minyaknya setiap hari.
6. Rematik
Bahan : Minyak jintan hitam
Cara : Hangatkan sedikit minyak jintan hitam, gosok secara perlahan di bagian tubuh yang terkena rematik. Untuk mempercepat penyembuhan, minum 1 sendok teh minyak jintan hitam 3 kali sehari.
7. Alergi
Bahan : Minyak jintan hitam
Cara : Minum 1 sendok teh minyak jintan hitam 2 kali sehari.
8. Hipertensi
Bahan : Biji jintan hitam, bawang putih, air panas.
Cara : Masukkan 1 sendok teh jintan hitam ke dalam air panas dengan 2 ptotong bawang putih. Minum airnya setiap pagi sebelum sarapan.
9. Sakit gigi
Bahan : Cuka apel, jintan hitam
Cara : Didihkan 8 ons cuka apel dan 2 sendok teh biji jintan hitam. Ramuan tersebut dipakai untuk kumur-kumur sampai sakitnya hilang.
10. Asma
Bahan : Minyak jintan hitam
Cara : Oleskan minyak jintan hitam di dada dan punggung. Atau campurkan 1 sendok teh minyak jintan hitam ke dalam air mendidih dan hirup uapnya dua kali sehari.
11. Kanker
Bahan : 2-3 g biji jintan hitam, masing-masing 10 g daun sambiloto, temulawak, kunyit, temu putih, temu mangga, ciplukan dan meniran.
Cara : Cuci bersih temulawak, kunyit, temu putih, temu mangga, lalu parut. Hasil parutan tadi dicampur dengan ciplukan, meniran, daun sambiloto. Rebus dengan 2 gelas air hingga tersisa 1,5 gelas. Hancurkan biji jintan hitam hingga halus. Selanjutnya campurkan bubuk biji jintan hitam ke dalam ramuan. Minum ramuan 3 kali sehari, masing-masing 1/2 gelas
Semoga berkenan
Posted by #rakmutublas

Rabu, 20 Juli 2011 - Selain senyawa kecil monomer, jenis senyawa organik lain telah disintesis dari kondisi Bumi purba. Senyawa ini antara lain asam dikarboksilik dan trikarboksilik, asam lemak, dan alkohol lemak. Namun untuk beraneka monomer biokimia, tidak ada sintesis dalam kondisi prebiotik yang dapat berlangsung yang berhasil ditunjukkan.
Di antara monomer ini adalah arginin, lisin, histidin, tiamin, asam folik, asam lipoik, biotin, dan piridoksal. Mungkin kalau sebagian senyawa ini pada kenyataannya tidak di sintesis di Bumi prebiotik, dan kalau keberadaannya dalam sistem kehidupan adalah hasil dari evolusi metabolik intrasel yang masih muda.
Dengan keahlian yang cukup dan kondisi eksperimental yang tepat, secara teoritis mungkin untuk mensintesis hampir semua jenis molekul organik. Sehingga sintesis non biologis dari sejumlah besar komponen monomer sel modern dalam kondisi laboratorium tidak bermakna kalau komponen-komponen ini esensial bagi asal usul kehidupan; tidak pula kalau itu berarti bahwa ia harus ada dalam lingkungan prebiotik. Dunia pra kehidupan purba mungkin merupakan dunia impian kimia, namun ia dapat tidak mencakup semua senyawa dan struktur molekul yang ditemukan dalam mikroba paling sederhana yang ada di masa kini.
Dasar utama teori asal usul kehidupan heterotropik adalah perawatan dan reproduksi sistem kehidupan pertama tergantung pada molekul organik yang disintesis secara prebiotik. Pembahasan mengenai bagaimana dunia primitif dibentuk sangat ramai dan panas. Apakah terlalu banyak tukang masak yang membuat supnya kacau?
Jelas tidak. Sungguh, sangat tidak mungkin kalau satu mekanisme dapat bertanggung jawab atas sejumlah besar senyawa organik yang harus ada dalam lingkungan primitif. Justru, sup prebiotik hampir pasti terbentuk oleh sumbangan sumber endogen dan eksogen – dari sintesis rumah tinggal dalam atmosfer reduksi dan pada sulfida logam di ventilasi dasar laut dalam, serta dari komet, meteorit, dan debu antar planet. Pandangan eklektis ini tidak menuntut isu signifikansi reltif berbagai kontributor senyawa organik: ia semata mengakui sejumlah besar sumber potensial bahan baku yang dibutuhkan untuk kemunculan kehidupan.
Keberadaan mekanisme non biologis yang beraneka ragam yang mana monomer yang relevan secara biokimia dapat di sintesis dalam kondisi prebiotik yang berhasil telah diterima luas. Tentu saja, tidak semua jalur prebiotik sama efisiennya, namun sejumlah besar kondisi eksperimen dimana senyawa organik dapat disintesis menunjukkan kalau sintesis prebiotik balok pembangun kehidupan itu baku. Reaksi abiotik yang menghasilkan senyawa demikian merentang luas dalam sejumlah latar; mereka tidak terbatas pada spektrum sempit kondisi reaksi selektif. Gagasan Miller dan Lazcano mengenai pembentukan senyawa organik secara prebiotik ini berdasarkan eksperimen dalam sistem model. Kebakuan pendekatan ini didukung fakta kalau meteorit karbonat mengandung sebagian besar jenis senyawa yang sama yang dihasilkan di lab. Perbandingan demikian menunjukkan kalau sangat mungkin sintesis organik nonbiologis yang sama terjadi di Bumi primitif. Walaupun banyak ketidakpastian di sekitar kemunculan kehidupan, pembentukan sebuah sup organik purba adalah salah satu peristiwa paling dipahami dalam sejarah Bumi.
Sumber
Miller, S.l., Lazcano, A. 2002. Formation of the Building Blocks of Life. Dalam Life’s Origin : The Beginnings of Biological Evolution. J. William Schopf. University of California Press, Ltd. hal. 78-112
referensi : faktakimia.com
Posted by #rakmutublas
ZAT ADIKTIF

Untuk mempertahankan hidupnya, manusia tidak lepas dari makanan. Guna makanan untuk mendapatkan energi, memperbaiki sel-sel yang rusak, pertumbuhan, menjaga suhu dan menjaga agar badan tidak terserang penyakit, makanan yang bergizi merupakan makanan yang mengandung karbohidrat, lemak, protein, vitamin, mineral dan air. Untuk maksud tersebut kita memerlukan zat aditif.
Zat aditif pada makanan adalah zat yang ditambahkan dan dicampurkan dalam pengolahan makanan untuk meningkatkan mutu. Jenis-jenis zat aditif antara lain pewarna, penyedap rasa, penambah aroma, pemanis, pengawet, pengemulsi dan pemutih.
Zat aditif pada makanan ada yang berasal dari alam dan ada yang buatan (sintetik). Untuk zat aditif alami tidak banyak menyebabkan efek samping. Lain halnya dengan zat aditif sintetik.
Bahan pengawet
Pengawet adalah bahan yang dapat mencegah atau menghambat fermentasi, pengasaman atau penguraian lain terhadap makanan yang disebabkan mikroorganisme. Zat pengawet dimaksudkan untuk memperlambat oksidasi yang dapat merusak makanan. Ada dua jenis pengawet makanan yaitu alami dan sintetik (buatan). Pengawet yang paling aman adalah bahan-bahan alam, misalnya asam cuka (untuk acar), gula (untuk manisan), dan garam (untuk asinan ikan/telur). Selain itu beberapa bahan alam misalnya saja penambahan air jeruk atau air garam yang dapat digunakan untuk menghambat terjadinya proses reaksi waktu coklat (browing reaction) pada buah apel.
Keuntungan zat aditif
Penggunaan zat aditif memiliki keuntungan meningkatkan mutu makanan dan pengaruh negatif bahan tambahan pangan terhadap kesehatan.
Agar makanan dapat tersedia dalam bentuk yang lebih menarik dengan rasa yang enak, rupa dan konsentrasinya baik serta awet maka perlu ditambahkan bahan makanan atau dikenal dengan nama lain “food additive”.
Penggunaan bahan makanan pangan tersebut di Indonesia telah ditetapkan oleh pemerintah berdasarkan Undang-undang, Peraturan Menteri Kesehatan dan lain-lain disertai dengan batasan maksimum penggunaannya. Di samping itu UU Nomor 7 tahun 1996 tentang Pangan Pasal 10 ayat 1 dan 2 beserta penjelasannya erat kaitannya dengan bahan tambahan makanan yang pada intinya adalah untuk melindungi konsumen agar penggunaan bahan tambahan makanan tersebut benar-benar aman untuk dikonsumsi dan tidak membahayakan.
Namun demikian penggunaan bahan tambahan makanan tersebut yang melebihi ambang batas yang ditentukan ke dalam makanan atau produk-produk makanan dapat menimbulkan efek sampingan yang tidak dikehendaki dan merusak bahan makanan itu sendiri, bahkan berbahaya untuk dikonsumsi manusia. Semua bahan kimia jika digunakan secara berlebih pada umumnya bersifat racun bagi manusia. Tubuh manusia mempunyai batasan maksimum dalam mentolerir seberapa banyak konsumsi bahan tambahan makanan yang disebut ADI atau Acceptable Daily Intake. ADI menentukan seberapa banyak konsumsi bahan tambahan makanan setiap hari yang dapat diterima dan dicerna sepanjang hayat tanpa mengalami resiko kesehatan.
ADI dihitung berdasarkan berat badan konsumen dan sebagai standar digunakan berat badan 50 kg untuk negara Indonesia dan negara-negara berkembang lainnya. Satuan ADI adalah mg bahan tambahan makanan per kg berat badan. Contoh: ADI maksimum untuk B-karoten = 2,50 mg/kg, kunyit (turmerin) = 0,50 mg/kg dan asam benzoat serta garam-garamnya = 0,5 mg/kg.
Untuk menghitung batas penggunaan maksimum bahan tambahan makanan, digunakan rumus sebagai berikut
BPM = ADIxB x1.000 / K (mg / kg)
Di mana BPM = batas penggunaan maksimum (mg/kg)
B = berat badan (kg)
K = konsumsi makanan (gr)
Contoh: Hitung BPM bahan tambahan makanan yang mempunyai ADI 2 mg untuk konsumsi makanan harian yang mengandung bahan tersebut (1 kg) dan bobot badan 60 kg ?
Jawab
BPM = ADIxB x1.000 / K (mg / kg)
= 2 x 60 x 1.000 /1.000
= 120 mg/kg
Jadi batas penggunaan maksimum bahan tambahan makanan yang mempunyai ADI 2 mg untuk 1000 gr makanan yang dikonsumsi konsumen yang berbobot 60 kg adalah 120 mg/kg. Perlu diingat bahwa semakin kecil tubuh seseorang maka semakin sedikit bahan tambahan makanan yang dapat diterima oleh tubuh.
Pada pembahasan berikut disajikan pengaruh negatif dan bahan tambahan pangan langsung yang meliputi: monosodium glutamat, sakarin dan siklamat, zat antioksidan, tartrazin, asam benzoat, kalium sorbat, natrium nitrit dan zat penambah gizi serta batasan penggunaan senyawa-senyawa tersebut yang aman bagi kesehatan manusia.
ikatan kovalen polar dan nonpolar VS molekul polar dan nonpolar
Pasangan elektron yang digunakan secara bersama pada pembentukan ikatan kovalen yang terletak diantara dua inti atom akan ditarik oleh kedua inti atom yang berikatan. Akibatnya akan mempengaruhi distribusi elektron di antara kedua inti yang berikatan. Kemampuan menarik elektron kearah dirinya tergantung pada keelektronegatifan masing-masing unsur yang berikatan.
Untuk molekul unsur, seperti H2, Cl2 dan N2 ikatan kovalen yang terbentuk seratus persen bersifat kovalen. Hal ini disebabkan kedua inti atom memiliki kemampuan yang sama untuk menarik elektron ke arah dirinya, sehingga elektron ikatan akan terdistribusi secara merata di antara kedua inti, seperti yang ditunjukan pada Gambar. Ikatan yang terbentuk dengan kemampuan menarik pasangan elektron yang sama kuat disebut ikatan kovalen nonpolar.

Gambar gambar Penyebaran elektron pada ikatan kovalen nonpolar Cl-Cl
Apabila kedua atom yang berikatan berbeda misalnya pada HF, HCl dan HI, maka ikatan yang terbentuk tidak sepenuhnya bersifat kovalen. Hal ini yang dinamakan ikatan kovalen polar. Dikatakan ikatan kovalen polar karena kedua atom yang berikatan terdapat gaya elektrostatik.

Gambar Ikatan kovalen polar C-Cl
Berdasarkan perbedaan kelektronegatifan, suatu ikatan kovalen dikatakan ikatan kovalen polar apabila suatu atom mampu menarik elektron ikatan ke arah dirinya tanpa melakukan perpindahan secara sempurna.
Semakin besar perbedaan keelektronegatifan unsur-unsur yang berikatan, semakin polar ikatan yang terbentuk bahkan mendekati sifat ionik. HX (X = Cl, Br, I, F), H2O, CO2, CCl4, BeCl2, BeCl3 dan NH3 merupakan beberapa contoh senyawa dengan ikatan kovalen polar. Misalnya HCl, meskipun atom H dan Cl sama-sama menarik pasangan elektron ikatan, tetapi keelektronegatifan Cl lebih besar dari atom H sehingga distribusi elektron ikatan lebih terkonsentrasi pada Cl.

Gambar ikatan kovalen polar H-Cl
Molekul Polar dan Nonpolar
Suatu senyawa yang memiliki ikatan kovalen polar, belum tentu molekul yang dimiliki bersifat polar. Demikian juga untuk ikatan kovalen nonpolar, molekul yang dimiliki belum tentu bersifat nonpolar. Kepolaran suatu molekul dinyatakan menggunakan suatu besaran yang disebut momen dipol (µ). Besarnya momen dipol suatu molekul ditentukan menggunakan persamaan berikut.
µ = Q x r 1 D = 3,33 x 10-30 C.m (coulombmeter)
µ = 0 → molekul nonpolar
µ > 0 atau µ ≠ 0 → molekul polar
keterangan:
µ = momen dipol (D, debye)
Q = selisih muatan (Coulomb)
r = jarak antara muatan positif dengan muatan negatif (m)
Semakin besar harga momen dipol, semakin polar senyawa yang bersangkutan bahkan mendekati ke sifat ionik. Harga momen dipol beberapa molekul seperti yang tertera pada Tabel.
molekul
Momen dipol (D)
molekul
Momen dipol (D)
NO
NH3
HF
HCl
HBr
HI
H2O
0,159
0,23
1,78
1,078
0,82
0,44
1,85
CO
CO2
CHCl3
CH4
CCl4
BF3
BF2
0,112
0
1,09
0
0
0
0
Momen dipol merupakan suatu besaran vektor yang digambarkan menggunakan moment ikatan. Jika jumlah vektor momen-momen ikatan lebih besar dari nol, maka molekul tersebut bersifat polar, sebaliknya jika jumlah vektor momen-momen ikatan sama dengan nol, maka maka molekul tersebut bersifat nonpolar.
Momen ikatan terbentuk jika dua atom yang berikatan dalam suatu senyawa memiliki perbedaan keelektronegatifan. Elektron yang yang ditarik oleh atom yang lebih elektronegatif menunjukan arah momen ikatan dan ditunjukan menggunakan tanda → dari atom yang kurang elektronegatif menuju atom yang lebih elektronegatif.
Akibat tarikan elektron yang terjadi, terbentuk semacam kutub negatif pada atom yang lebih elektronegatif, sedangkan pada atom yang kurang elektronegatif akan terbentuk semacam kutub positif.
Kutub positif atau negatif yang terbentuk disebut muatan parsial, yang digambarkan menggunakan simbol delta (δ). Muatan parsial negatif (δ¯) diberikan pada unsur yang lebih elektronegatif dan muatan parsial positif (δ+) diberikan pada unsur yang kurang elektronegatif (lebih elektropositif).
Berikut contoh menggambar muatan parsial pada molekul HCl.

Dari contoh di atas terlihat bahwa terdapat muatan positif dan negatif pada tanda δ yang digunakan. Tanda tersebut tidak sama dengan +1 atau -1 seperti pada simbol ion, tetapi tanda ini hanya menggambarkan elektron ikatan tidak sepenuhnya dipindahkan ke atom Cl.
Untuk senyawa diatom yang disusun oleh unsur yang sejenis, molekul yang dimiliki selalu bersifat nonpolar kecuali ozon yang bersifa polar. Hal ini disebabkan dua atom penyusun senyawa memiliki keelektronegatifan sama sehingga tidak terbentuk momen ikatan. Sedangkan untuk senyawa diatom yang disusun oleh dua atom yang berbeda molekul yang dimiliki selalu bersifat polar karena adanya perbedaan keeltronegatifan.
Tetapi untuk senyawa-senyawa yang tersusun lebih dari dua atom, kepolaran molekul tidak dapat ditentukan jika hanya didasarkan pada perbedaan keelektronegatifan. Hal ini disebabkan senyawa-senyawa tertentu walaupun memiliki ikatan kovalen polar tetapi molekulnya bersifat nonpolar. Misalnya CCl4, CO2 dan BeCl2 merupakan beberapa senyawa dengan ikatan kovalen polar tetapi memiliki molekul yang nonpolar.
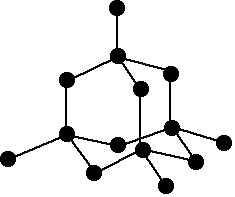
Pada molekul CCl4, yang mempunyai bentuk molekul tetrahedaral dengan C sebagai atom pusat dan dikelilingi oleh 4 atom Cl seperti pada Gambar.

Perbedaan keelektronegatifan C dan Cl adalah sebesar 3-2,5 = 0,5. Jadi ikatan C–Cl termasuk ikatan kovalen (tepatnya ikatan kovalen polar) karena perbedaan keeltronegatifan lebih kecil 1,7. Walaupun ikatan C–Cl berupa ikatan kovalen polar tetapi molekulnya bersifat nonpolar.
Hal ini disebabkan, bentuk tetrahedral dari molekul CCl4 dapat dikatakan simetrism karena memiliki pusat simetri pada atom C ditengah, sehingga jumlah momen ikatan yang sama dengan nol. Atau dapat dikatan tarikan elektron akibat adanya perbedaan keelektronegatifan saling meniadakan atau saling menguatkan (perhatikan tanda panah pada strutur). Hal ini dapat diandaikan, suatu benda yang berada di tengah-tengah ditarik dari empat sudut dengan kekuatan sama, maka benda tersebut tidak akan bergerak. Karena hal inilah molekul CCl4 bersifat nonpolar.
Jika CCl4 salah satu atom Cl diganti oleh atom lain misalnya H, maka sifat molekul yang awalnya nonpolar berubah menjadi polar. Hal ini disebabkan kepolaran ikatan C-H berbeda dengan kepolaran ikatan C-Cl, sehingga momen dipol yang terbentuk tidak saling meniadakan. Tetapi apabila semua atom C diganti oleh atom H maka molekulnya bersifat nonpolar karena kepolaran semua ikatan C–H sama besar sehingga mpmen ikatan yang terbentuk saling meniadakan.
Pada molekul BCl2 dan CO2 mempunyai bentuk molekul linear dengan B dan C sebagai atom pusat.

Atom Cl dan atom O lebih elektronegatif dibanding atom B dan C yang bertindak sebagai atom pusat (pada gambar yang berwarna hitam), sehingga elektron ikatan lebih tertarik kearah atom Cl dan O. Namun, atom B dan C masing-masing mengikat 2 atom yang sejenis maka momen ikatan yang terbentuk tertarik ke arah yang berlawanan dengan kekuatan yang sama, sehingga molekulnya bersifat nonpolar.
Molekul H2O walaupun rumus molekulnya mirip dengan CO2 dan BCl2 tetapi bersifat polar.

Hal ini disebabkan, pada molekul H2O, atom O sebagai atom pusat masih memiliki pasangan elektron bebas. Hal ini menyebabkan molekul H2O tidak berbentuk linear seperti molekul CO2 dan BCl2, sehingga momen ikatan yang terbentuk tidak saling menguatkan atau tidak saling meniadakan.
21 alasan mengapa kita menyayangi bakteri...

Beberapa jenis bakteri di dalam saluran pencernaan mmbantu memecah makanan sehingga mudah diserap dan diambil nutrisinya bagi tubuh.
#
Bakteri probiotik membantu mncegah racun yang ada dalam pencernaan terserap ke pembuluh darah dan mngendalikan jumlah bakteri jahat.
#
Bakteri probiotik juga sangat bagus untuk menjaga kesehatan saluran pencernaan dan sistem kekebalan tubuh.
#
Osaka University School of Medicine : beberapa probiotik efektif untuk pengobatan kasus alergi pada hidung dan sinus.
#
Strain bakteri yang efektif utk pengobatan alergi : Lactobacilli casei, L. paracasei, L. acidophilus, dan Bifidobacterium longum.
#
Yakult Central Institute for Microbiological : bakteri tertentu dapat menekan respon peradangan/inflamasi pada tubuh.
#
University of British Columbia : probiotik dapat mencegah terjadinya radang usus besar dengan menjaga keseimbangan flora normal dalam usus besar.
#
University of Western Ontario : probiotik membantu mengurangi keluhan penderita rematik pada sendi.
#
University of Turku : terjadi peningkatan kandungan nutrisi pada ASI bila ibu menyusui mengkonsumsi suplemen probiotik.
#
Sapienza University : Lactobacillus brevis memiliki kemampuan sebagai antivirus untuk memerangi virus herpes simplex tipe 2.
#
Lactobacilli dan bifidobacteria memiliki kemampuan sebagai antioksidan untuk mencegah penuaan dini.
#
Probiotik mengurangi produksi hormon cytokines. Hormon ini meningkat pada kondisi depresi dan gangguan cemas.
#
International University of Health and Welfare Hospital : probiotik memperbaiki kondisi usus besar dan mencegah kanker usus besar.
#
American Journal of Clinical Nutrition : L. plantarum mengurangi stress oksidatif yang dapat menyebabkan gangguan pada syaraf dan otak.
#
Probiotik dapat menekan pertumbuhan bakteri helicobacter pylori yang berperanan saat terjadinya ulkus lambung/maag.
#
University Clinical Centre Tuzla : probiotik membantu memulihkan fungsi hati pada pasien pasca operasi kanker hati.
#
University of Alberta : probiotik mengurangi terjadinya komplikasi pada saluran cerna saat pasien dalam pengobatan kemoterapi.
#
Harvard Medical School : Lactobacillus acidophilus berguna dalam pencegahan dan pengobatan kanker usus besar.
#
Internal and Emergency Medicine : probiotik berguna untuk mencegah kegemukan dengan cara menjaga keseimbangan flora normal usus.
#
Jangan takut sekitar 1 triliun bakteri saat ini ada di pencernaan anda dan sebagian besar diantaranya sangat bermanfaat.
#
Fakta : jumlah mikroorganisme yang ada di dalam pencernaan jauh lebih banyak daripada jumlah sel tubuh.
Posted by #rakmutublas
Batuan Greenland dan Asal Usul Kehidupan

Bumi berusia 4,5 miliar tahun. Ini fakta yang cukup handal. Usia dari banyak batuan purba juga handal, dan mereka berusia sangat tua: ada batuan di Greenland yang berusia 3,8 miliar tahun. Tanda pertama kehidupan dalam batuan purba tidak dapat dengan mudah diketahui apalagi ditentukan usianya, namun ada bukti yang baik sekarang kalau sejenis mikroba telah ada setidaknya 2,8 miliar tahun lalu. Ini perkiraan yang sangat hati-hati; sebagian besar pakar akan mengatakan kalau sekarang telah ada bukti kalau ada kehidupan di Bumi 3,5 miliar tahun lalu. Beberapa diantaranya bahkan menarik waktunya lebih jauh hingga 3,8 miliar tahun.
Bukti paling langsung ada dua. Pertama ada struktur berskala besar yang tidak biasa dalam banyak batuan purba, termasuk batuan Australia kuno berusia 3,5 miliar tahun, yang mirip dengan struktur stromatolit yang di masa sekarang diproduksi oleh koloni mikroba dalam jumlah besar. Dan kedua, ada benda-benda yang ditemukan di batuan purba yang tampaknya merupakan fosil dari mikroba itu sendiri.
Bergerak ke ujung lain jangkauan waktu asal usul kehidupan di Bumi, waktu tertua yang mungkin dipastikan oleh usia Bumi itu sendiri, namun ada bukti dari Bulan dan banyak planet lain kalau Bumi di bombardir oleh meteorit-meteorit sangat besar hingga sekitar 4,0 miliar tahun lalu. Jadi ujung jauh dari jangkauan asal usul kehidupan mungkin lebih dekat ke 4,0 ketimbang 4,5 miliar tahun lalu. Di sisi lain, atau sisi pesimis, waktu asal usul kehidupan termuda adalah 2,8 miliar tahun dan ujung dekat ini tampaknya akan semakin terdorong jauh berkat penemuan-penemuan baru. Jadi, mungkin gapnya akan menyempit. Namun untuk sementara kita dapat tenang dengan jangkauan waktu 4,5 (atau kurang) hingga 2,8 (atau lebih) miliar tahun lalu untuk asal usul kehidupan di Bumi.
Untuk kondisi Bumi ketika kehidupan bermula, bukti terbaik yang kita miliki adalah yang datang dari batuan Greenland tadi, 3,8 miliar tahun lalu. Waktu tersebut berada dalam jangkauan asal usul kehidupan kita. Batuan itu sendiri berbicara kalau Bumi tidak terlalu berbeda dari sekarang. Batuan ini dulunya adalah endapan: mereka terbaring di dasar perairan yang luas. Dan mungkin ada daratan juga, untuk menyediakan bahan untuk diendapkan. Batuan Greenland mengandung karbonat – jadi mungkin ada karbon dioksida di atmosfer – dan juga terdapat endapan-endapan mengandung besi yang paling mungkin, hanya dapat terbentuk ketika tidak ada ataupun hanya ada sedikit oksigen di atmosfer. Dan umumnya diduga kalau juga ada nitrogen di atmosfer purba untuk menjadi penyusun utamanya seperti sekarang.
Pendapat lain mengatakan kalau atmosfer purba Bumi mirip dengan Yupiter. Namun pendapat kalau atmosfer purba kita berat, penuh metana, amonia, dan segala kawanannya ini tidak didukung oleh bukti dari batuan purba; dan sedikit pula antusiasme atas gagasan ini sekarang, baik diantara para geolog, geokimiawan, ataupun astronom planet.
Sumber
Cairns-Smith, A.G. 2000. Seven Clues to the Origin of Life. Cambridge University Press.
referensi dari faktakimia.com
Posted by #rakmutublas
kandungan asap rokok....!!

Kamis, 10 Maret 2011 - Kandungan rokok dapat ditentukan lewat dua cara, langsung memeriksa rokoknya, atau memeriksa asapnya. Asap rokok sendiri ada dua jenis : Asap yang keluar dari pembakaran di ujung rokok dan asap yang dihirup oleh perokok lewat ujung hisap rokok (baik filter atau tidak). Pembahasan berikut hanya mengenai zat yang terkandung dalam asap rokok saja (tanpa melihat ujung mana yang mengeluarkan asap).
Ada bukti konklusif kalau tar yang terkandung dalam asap rokok dapat menyebabkan kanker paru; faktor utamanya adalah usia individu saat mulai merokok, kedalaman hisapan dan jumlah rokok yang dikonsumsi per hari. Polonium, sebuah unsur radioaktif, juga diketahui hadir dalam asap rokok; lebih dari 100 senyawa telah ditemukan termasuk nikotin, cresol, karbon monoksida, pyridene dan benzopyrene, yang terakhir ini adalah zat karsinogen (penyebab kanker).
Walau ada 100 lebih senyawa, berikut senyawa-senyawa penting saja yang dibahas.

Ammonia
Rumus molekul NH3. Umumnya digunakan untuk pupuk dan pada pabrik serat dan perantara plastik. Sudah dikenal semenjak zaman purba. Pada suhu dan tekanan standar, NH3 adalah gas yang tidak berwarna dengan bau menusuk bila dalam konsentrasi kecil. Dalam konsentrasi besar, mampu menghasilkan sensasi ketika dihirup.
Arsen
Senyawa kimia dengan simbol As. Nomor atom 33. Menyublim bila dipanaskan dan tidak berubah pada udara yang kering, namun film oksida terbentuk di udara lembab. Bila dipanaskan pada suhu 180 derajat Celsius di udara membentuk arsenik trioksida yang berbau bawang putih dan beracun.
Butana
Rumus molekul C4H10. Merupakan salah satu jenis hidrokarbon asiklik jenuh. Toksisitas rendah.
Cadmium
Unsur kimia dengan simbol Cd dan nomor atom 48. Selalu berasosiasi dengan seng walaupun hanya menyusun 0.15 bpj kerak bumi di urutan ke 57. Memiliki sifat racun, khususnya dalam bentuk serbuk dan potongan. Manfaat utamanya adalah untuk memperkuat daya tahan baja terhadap karat.
Karbon Monoksida
Rumus molekul CO, merupakan jenis oksida karbon. Merupakan senyawa karbon inorganik. Merupakan hasil pembakaran tidak sempurna karena hanya memuat satu atom oksigen. Ditemukan dalam asap knalpot. Tidak berbau dan tidak berwarna namun sangat beracun. Afinitasnya terhadap hemoglobin darah 300 kali lebih kuat dari oksigen sehingga paparan gas ini dapat mengurangi atau sepenuhnya menghilangkan kemampuan hemoglobin mengangkut oksigen ke seluruh tubuh, menyebabkan kematian bila dalam konsentrasi tinggi.
Hydrogen Sianida
Rumus kimia HCN. Sangat beracun. Merupakan hasil dari reaksi amonia, metana, oksigen dan nitrogen.
Metanol
Nama lainnya metil alkohol. Rumus kimia CH3OH. Saat terbakar, metanol memiliki asap biru dengan api transparan. Pengaruh terbesar pada selaput lendir. Dalam tubuh, produk ini terbentuk oleh oksidasi dengan formaldehida dan asam formik, keduanya beracun.
Naphthalene
Senyawa ini adalah turunan dari tar batu bara. Merupakan hasil dari distilasi tar mentah menjadi minyak kimia. Pemberian larutan caustik pada minyak kimiawi menghasilkan lapisan minyak. Lapisan minyak kemudian diberi larutan asam sehingga menjadi lapisan minyak netral. Lapisan minyak netral kemudian di distilasi dan produk akhirnya adalah naphthalene.
Phenol
Rumus kimia C6H5OH, nama lainnya asam karbolik, asam fenilik, benzofenol atau hidroksibenzena. Merupakan senyawa hidroksi aromatik paling sederhana. Phenol juga merupakan petrokimia paling penting. Biasa digunakan untuk pelapis triplek. Ia memiliki bau khas dan rasa terbakar yang tajam. Beracun bila dihirup, dicerna atau diserap oleh kulit. Ia juga mengakibatkan iritasi. Bila ada dalam larutan yang sangat lemah, ia akan terasa manis.
Polonium – 210
Isotop dari unsur kimia Polonium. Merupakan isotop Polonium paling stabil dalam deret radioaktif Uranium dengan waktu paruh (half life) 138,4 hari. Muncul secara alamiah hanya sebagai hasil peluruhan dari thorium dan uranium.
Toluena
Rumus kimia C7H8. Umum diproduksi bersama dengan bensin, xylena, dan aromatik C9 lewat pembentukan ulang katalitik C6-C9 naphtha.
Uretan
Rumus kimianya adalah CO(NH2)OC2H5, yang disebut juga etil karbamat atau etil uretan. Terbentuk karena pemanasan etanol dan urea nitrat pada suhu 120-130 derajat Celsius atau karena tindakan amonia pada etil karbonat atau etil kloroformat.
Vinyl klorida
Rumus kimia CH2=CHCl. Pengaruh terbesarnya ada pada kulit manusia yang dapat menyebabkan sindrom Raynaud, lisis tulang distal di jari dan dermatitis fibrosa. Menghirup gas vinyl klorida selama bertahun-tahun dapat menyebabkan jenis kanker hati yang langka, angiosarkoma. Vinyl klorida digunakan sebagai bahan dasar pembuatan plastik PVC.
Referensi
Van Nostrand’s Encyclopedia of Science
Inovasi Terbaru Menuai Hidrogen dari Air

Usaha para ilmuwan dalam mencari energi alternatif pengganti bahan bakar fosil terus dilakukan, terutama sejak memasuki abad ke-21 ini. Hingga saat ini persentase penggunaan energi alternatif masih sangat sedikit dikarenakan efektivitas dan efisiensinya yang tergolong masih kecil. Hal seperti ini juga tampak pada penggunaan bahan bakar hidrogen. Meski beberapa perusahaan otomotif seperti Ford dan Honda telah merilis mobil berbahan bakar hidrogen, pada kenyataannya penggunaannya masih sedikit. Problema ini tak lepas dari mahalnya hidrogen cair karena biaya produksinya yang dapat dikatakan tidak murah.
Hidrogen memiliki banyak kelebihan, antara lain memiliki energi pembakaran yang besar per satuan massa hidrogen dan merupakan bahan bakar yang sangat bersih karena emisi pembakarannya berupa air (H2O). Baru-baru ini, tim peneliti dari School of Chemistry Monash University Australia telah menemukan inovasi baru dalam mengubah air menjadi hidrogen lewat proses elektrofotokatalisis yang terinspirasi dari cara tumbuhan mengubah air menjadi oksigen.
Para ilmuwan di dunia mengakui bahwa bagian tersulit dari mengubah air menjadi bahan bakar adalah mengonversi air menjadi hidrogen dan oksigen. Tim peneliti yang telah mempublikasikan hasil penelitian mereka di jurnal Nature Chemistry ini berhasil membuat sistem sel konversi air menjadi hidrogen menggunakan katalis berbasis logam mangan (Mn). Katalis ini sendiri memiliki struktur molekul yang menyerupai mineral mangan birnessite [(Na0.3Ca0.1K0.1)(Mn4+,Mn3+)2O4 · 1.5 H2O].
Tim peneliti tersebut memanfaatkan tingkat oksidasi dari ion mangan, terutama mangan (II) dan mangan (IV) untuk mengoksidasi air menjadi oksigen dan hidrogen. Pemberian tegangan listrik akan mengubah mangan (II) pada birnessite teroksidasi menjadi mangan (IV). Selanjutnya pemaparan dengan cahaya matahari akan mengembalikan bentuk mangan (IV) menjadi mangan (II) sekaligus mengubah dua molekul air (H2O) menjadi satu molekul gas oksigen (O2), empat proton (H+), dan empat elektron. Selanjutnya keempat proton dan elektron tersebut bergabung menjadi dua molekul gas hidrogen (H2). Siklus katalis mangan berlangsung cepat dan voltase listrik yang dibutuhkan tidak terlalu besar jika dibandingkan dengan elektrolisis langsung air menggunakan elektroda inert.
Inovasi ini terbukti menghasilkan gas hidrogen dari air secara lebih mudah dan murah. Penemuan ini diharapkan akan menginspirasi produsen bahan bakar hidrogen di dunia untuk mengaplikasikannya sehingga akan terwujud penggunaan bahan bakar hidrogen yang mengglobal.
Posted by #rakmutublas
Penjelasan mengenai akumulasi asam di atmosphere

Beberapa studi baru mungkin dapat membantu menjelaskan konsentrasi tinggi dari asam sulfuric di atmosphere. Penelitian ini dapat juga memberikan implikasi bagi pemodelan cuaca global, yang memungkinkan para ilmuwan untuk mengurangi ketidak menentuan yang berkaitan dengan efek aerosol berdasarkan prediksi mereka.
Para ilmuwan telah berusaha bertahun-tahun untuk merekonsiliasikan konsentrasi atmospheris dari asam sulfuric yang merupakan hasil dari eksperimen laboratorium terhadap tingkat formasi partikelnya. Menurut Mikko Sipilä dari University of Helsinki di Finlandia, hal ini menurun pada ketidak cukupannya pendetektor partikel pada eksperimen sebelumnya – salah satu yang terbaik hanya mampu mendeteksi partikel sebesar 3nm dan diatasnya. Namun sekarang ini Sipilä dan sebuah tim dari peneliti internasional telah mengembangkan beberapa metode untuk mendeteksi partikel yang hampir lebih besar dari nanometer tunggal.
Sebagaimana penjelasan Sipilä, pada konsentrasi dibawah 108 molekul per kubik sentimeter, yang berada di atmosphere, partikel asam sulfuric yang dibentuk oleh kondensasi dari gas H2SO4 tumbuh sangat lamban sekali. ‘Ini berarti bahwa didalam waktu mendiami yang digunakan pada studi sebelumnya – secara tipikal beberapa puluh detik – beberapa partikel tidak dapat tumbuh diatas batas deteksi partikelnya yang berlawanan dengan apa yang mereka sedang dunakan,’ katanya.
Dengan menggunakan metode deteksi yang telah dikembangkan, para peneliti menunjukkan bahwa tidak adanya ketidak sesuaian dari beberapa aturan besaran gayanya antara tingkat yang diamati dan perkembangan teoritisnya. Sementara tingkat perkembangan yang mereka lakukan tidaklah sesuai dengan prediksi sebelumnya dari teori tersebut, mereka mengatakan bahwa persetujuannya adalah ‘baik’.
Pada teori nukleasi, adanya ambang penerimaan yang kritis dimana beberapa partikel seperti asam sulfuric menjadi stabil saat mereka mengkondensasi. Para peneliti mengungkapkan bahwa nukleus yang kritis di kasus ini berisi satu hingga dua molekul asam sulfuric. Namun Renyi Zhang, seorang ahli pada ilmu pengetahuan atmospheris pada Texas A&M University di Amerika Serikat, mengatakan bahwa ‘hal ini sangatlah sulit untuk menjelaskan bagaimana satu hingga dua molekul asam sulfuric, bersama –sama dengan molekul air, dapat membuat suatu nukleus yang kritis, dari sudut pandang thermodinamika.’ Dia menambahkan bahwa hasilnya masih perlu direproduksi lagi oleh kelompok lainnya.
Jika hasilnya direproduksi kembali, bagaimanapun juga, mereka mungkin mempunyai implikasi yang penting bagi ilmu pengetahuan cuaca. Sipilä menjelaskan bahwa efek tidak langsung dari aerosol merupakan beberapa hal yang sedikit dapat dipahami dengan baik dalam model cuaca. ‘Akhir-akhir ini Saya pikir pada beberapa model tersebut yang digunakan untuk laporan [Intergovernmental Panel on Climate Change], nukleasinya baik diacuhkan sepenuhnya ataupun hal ini barangkali didasarkan pada pengamatan ambien,’ says Sipilä. ‘Jika saja langkah molekular yang detail tidak diketahui maka hal ini akan menciptakan banyaknya ketidak pastian pada model tersebut. Oleh karena itu mengapa hal ini sangatlah penting untuk memahami langkah yang detail yang nantinya akan meningkatkan akurasi prediksi cuaca global.’
Hayley Birch
Referensi
M Sipilä et al, Science, 2010, DOI: 10.1126/science.1180315
Posted by #rakmutublas
Evolusi Mikroorganisme di Laut Mati

Mikrobiologis dari Institute of Biology II University of Freiburg telah menemukan suatu jalur metabolisme sentral dari mikroorganisme yang sebelumnya tidak diketahui.
Mikroorganisme ekstremofil (extremophile) atau mikroorganisme yang biasa hidup di tempat-tempat ekstrem ini menggunakan jalur metabolisme ini untuk dapat bertahan hidup di tempat-tempat ekstrem seperti halnya Laut Mati yang salinitasnya sangat tinggi.
Bertentangan dengan anggapan yang popoler di masyarakat, Laut Mati tidaklah mati. Laut Mati yang berada di antara Yordania dan Israel ini berisi berbagai macam populasi mikroorganisme. Kebanyakan mikroorganisme ini termasuk dalam kelompok archaea yang toleran terhadap kadar garam tinggi. Archaea merupakan salah satu bentuk kehidupan yang paling awal terbentuk di muka bumi dan mampu bertahan hidup pada kondisi ekstrem. Tim riset di Freiburg yang dikepalai oleh Dr. Ivan Berg telah mempelajari proses metabolisme mikroorganisme ini yang sebelumnya selalu dihindari oleh ahli biologi evolusi.
Ilmuwan telah lama mengetahui bahwa archaea yang toleran terhadap salinitas tinggi menggunakan berbagai macam senyawa organik sebagai sumber nutrisi mereka yang kemudian digunakan untuk mensintesis pelindung dinding sel dan vitamin yang teraktivasi asam asetat (asetil koenzim A). dengan menggunakan mikroorganisme Haloarcula marismortui sebagai model, Dr. Ivan Berg bersama koleganya di Freiburg Dr. Maria Khomyakova, Özlem Bükmez, Lorenz Thomas, dan Dr. Tobias Erb telah berhasil menguraikan secara detil jalur metabolisme mikroorganisme tersebut. Kabar terbaru dari jurnal Science, para peneliti menjelaskan bagaimana mereka dapat mengetahui keseluruhan siklus reaksi, termasuk seluruh intermediet yang terbentuk, dengan berbagai bantuan metode biokimia dan mikrobiologi. Tim ini memberi nama jalur metabolisme lengkap ini sebagai “siklus metilaspartat” setelah mengkarakterisasi zat antara yang penting dalam siklus tersebut.
Grup riset Freiburg ini belum mengetahui awal terjadinya jalur metabolisme seperti ini dan diperkirakan merupakan salah satu bentuk evolusi dari pendahulunya yang harus menemukan jalur metabolisme tersendiri demi beradaptasi dengan habitatnya yang berkadar garam sangat tinggi. Para peneliti ini juga terkejut saat menemukan bahwa gen leluhur archaea yang mengandung informasi jalur metabolisme ini didapat dari mikroorganisme lain.
Fenomena transfer gen antar-organisme ini sekarang biasa dikenal sebagai “transfer gen bercabang”. Bagaimanapun, ilmuwan belum mengobservasi gen terdahulu yang mengandung informasi siklus metilaspartat dan digolongkan sebagai jalur metabolisme yang benar-benar baru. Kemungkinan, rekombinasi gen lelulur archaea mengarah kepada jalur metabolisme ini. Para peneliti menyatakan bahwa lebih sulit untuk menemukan sebuah gen baru dibandingkan dengan mengkombinasikan gen-gen yang sudah ada.
Posted by #rakmutublas
Kemotaksis Droplet Acidic memecahkan teka – teki

Manufer teka – teki suatu perjalanan droplet melalui jalan berliku dengan gradien pH. Pada gambar hamparan, tetesan hitam menunjukkan waktu awal, sedangkan yang merah adalah kelanjutannya.
Dalam dunia keilmiahan, memecahkan teka – teki dulunya merupakan ranah dari eksperimen pesikologi. Sekarang ini ahli kimiawi mulai bertindak, tetapi mereka menyingkirkan tikus percobaan yang kuno dengan suatu tetesan cairan. Sebuah tim yang dipimpin oleh profesor ilmu kimia pada Universitas Northwestern yaitu Bartosz A. Grzybowski telah menunjukkan bahwa suatu droplet acidic dapat menavigasi dengan sukses suatu teka – teki yang komplek (J. Am. Chem. Soc., DOI: 10.1021/ja9076793).
“Saya secara pribadi menemukan sesuatu yang paling menggembirakan bahwa suatu sistem yang sederhana dapat menunjukkan tingkah laku yang kelihatannya ‘pandai’,” komentar profesor John A. Pojman dari Louisiana State University. “Pendekatan ini sangat berguna sebagai metode pemompa bagi mikrofluida atau suatu cara untuk mengubah energi kimia menjadi gerakan mekanis pada peralatan yang kecil. Saya ingin sekali melihat jika mereka dapat mengeneralisasikanhal ini kepada tipe gradien lainnya,” katanya.
Droplet, yang tersusun dari asam 2-hexyldecanoic baik pada dichloromethane atau minyak mineral, berjalan beberapa sentimeter melalui suatu teka – teki dengan gradien pH. pH ini sangat tinggi pada pintu masuk teka – tekinya dan rendah pada pintu keluarnya. Saat berada di teka – teki, droplet ini berjalan menuju pH yang rendah, dan selanjutnya begitu terus, jelas Grzybowski, ini selalu menemukan jalan yang pendek melalui teka – teki ini.
Kimiawi asam-basa dan tensi permukaannya adalah apa yang mendorong tetesan tersebut. “Reaksi interfasial antara asam pada tetesan tersebut dengan basa di salurannya menciptakan konfeksi gulungan atau ‘pilinan,’” terang Grzybowski. “Mekanik fluida memerankan hal itu bahwa pilinan yang menghadap pH yang lebih rendah lebih dinyatakan, dan sehingga tetesan tersebut secara efektif mendorong pada suatu arah.”
Posted by #rakmutublas
Pemanasan Global Meningkatkan Kapasitas Pohon Untuk Menyerap Karbon

Saat ini pemanasan global telah berada pada tingkat yang semakin mengkhawatirkan hingga diperlukan langkah-langkah untuk mencegah dan menguranginya. Salah satu cara yang paling efektif adalah dengan menanam lebih banyak pohon dan melindungi hutan. Pohon dan tetumbuhan lainnya menyerap karbon dioksida selama proses fotosintesis. Proses ini mampu mengurangi gas rumah kaca yang paling melimpah di atmosfer tersebut dan menyimpannya di dalam jaringan kayu.
Suatu riset terbaru yang dipimpin oleh Jerry Melillo dari Marine Biological Laboratory (MBL) selama 7 tahun memperlihatkan bahwa pemanasan global dapat mempengaruhi kapasitas penyimpanan karbon dari pohon. Studi ini dilakukan di hutan Harvard tengah kota Massachussets dengan luas sekitar seperempat acre (sekitar 1000 m2). Hutan ini dihangatkan secara buatan sekitar 9°F di atas suhu normal untuk mensimulasikan keadaan pemanasan global dan respon tumbuhan terhadap kondisi tersebut.
Studi sebelumnya menjelaskan bahwa naiknya temperatur tanah dapat meningkatkan dekomposisi materi organik tanah sehingga pelepasan karbon dioksida juga meningkat. Tetapi studi ini juga menunjukkan bahwa temperatur yang lebih hangat menstimulasi tumbuhan untuk menyerap lebih banyak karbon sebagai jaringan kayu. Hal tersebut dipengaruhi oleh senyawa nitrogen yang terbentuk saat temperatur tanah meningkat. Sebagian besar hutan di daerah subtropis hingga sedang, seperti di daerah Amerika Utara, Eropa, dan Eurasia kekurangan senyawa nitrogen untuk tumbuh kembangnya. Sehingga dengan meningkatnya senyawa nitrogen yang diserap tumbuhan dapat mempercepat pertumbuhannya.
Pemanasan pada tanah membuat senyawa nitrogen yang terdapat pada materi organik tanah terlepas sebagai senyawa nitrogen anorganik seperti ammonium. Ammonium merupakan komponen utama yang terdapat pada pupuk buatan. Ketika tumbuhan menyerap senyawa nitrogen anorganik ini pertumbuhannya akan semakin cepat dan mampu menyerap lebih banyak karbon.
Proses biologis yang menghubungkan pemanasan tanah, meningkatnya penguraian materi organik, peningkatan senyawa nitrogen, dan peningkatan pertumbuhan pohon terlihat berhubungan erat untuk hutan daerah subtropis. Namun hasil studi ini kurang relevan diterapkan untuk hutan tropis karena studi ini dilakukan di daerah hutan subtropis yang kekurangan nitrogen. Sementara hutan tropis melimpah akan senyawa-senyawa nitrogen.
Posted by #rakmutublas








